2024年1月北京各区高中期末考试陆续落下帷幕,为了更好的帮助大家复盘,利用寒假备考复习,查缺补漏。北京高考在线为大家整理了2024高考化学氧化还原反应的基本规律!希望对大家高中化学答题及备考有帮助!
2024高考化学氧化还原反应的基本规律
1、守恒规律
还原剂失电子总数=氧化剂得电子总数=氧化剂化合价降低的总数=还原剂化合价升高的总数。
应用:氧化还原反应方程式的配平和相关计算。
2、强弱规律
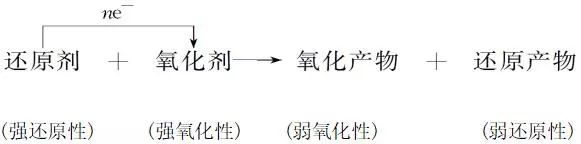
还原性:还原剂>还原产物。
氧化性:氧化剂>氧化产物。
应用:物质间氧化性(或还原性)的强弱比较或判断氧化剂和有还原性的物质在一定条件下是否发生反应。
3、先后规律
(1)同一氧化剂与多种还原剂混合,还原性强的先被氧化。
(2)同一还原剂与多种氧化剂混合,氧化性强的先被还原。
应用:判断物质的氧化性、还原性强弱或判断反应的先后顺序。
如:把氯气通入FeBr2溶液时,还原性Fe2+>Br-,若氯气的量不足时首先氧化Fe2+;把氯气通入FeI2溶液时,还原性I->Fe2+,若氯气的量不足时首先氧化I-。
4、价态规律
(1)高低规律
元素最高价态:只有氧化性。
元素中间价态:既有氧化性又有还原性。
元素最低价态:只有还原性。
应用:判断物质的氧化性、还原性。
(2)归中规律
①同种元素不同价态之间发生氧化还原反应时,高价态+低价态――→中间价态,即“只靠拢,不交叉”
②同种元素相邻价态间不发生化学反应。
应用:判断同种元素不同价态的物质间发生氧化还原的可能性。
(3)歧化规律
同种元素的中间价态生成高价和低价,即中间价―→ 高价+低价。
声明:本文由北京高考在线团队(微信公众号:bjgkzx)排版编辑,内容来源于网络,如有侵权,请及时联系管理员删除。




































