2023年北京各区高三期中考试已经落下帷幕,为了更好的帮助同学们复盘考试情况,查缺补漏。北京高考在线为大家整理了2024高考化学氧化性和还原性强弱的比较!希望对大家高中化学答题及备考有帮助!
2024高考化学氧化性和还原性强弱的比较
1、根据氧化还原反应方程式比较
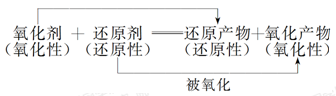
氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
2、根据元素的活动性顺序比较

3、根据反应条件来判断
当不同的氧化剂(或还原剂)与同一还原剂(或氧化剂)反应时,反应越易进行,则对应的氧化剂(或还原剂)的氧化性(或还原性)越强,反之越弱。如:
(1)
MnO2+4HCl(浓)=MnCl2+Cl2↑+8H2O
2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O
氧化性:KMnO4>MnO2。
(2)Na、Mg、Al单质与H2O反应情况如下,Na与冷水剧烈反应,Mg加热才反应,Al加热条件下也难反应,故还原性:Na>Mg>Al。
4、根据氧化产物的价态高低判断
当变价的还原剂在相似的条件下作用于不同的氧化剂时,可由氧化产物元素价态的高低来判断氧化剂氧化性的强弱。即在相同条件下,使还原剂价态升得越高,则氧化剂的氧化性越强。
【特别提醒】
(1)氧化性、还原性的强弱取决于物质得、失电子的难易程度,与得、失电子数目的多少无关。如:Na原子能失1个电子,Al可失3个电子,但根据金属活动性顺序表,Na比Al活泼,更易失去电子,所以Na比Al的还原性强。
(2)对同一元素而言,一般价态越高,氧化性越强,如Fe3+>Fe2+>Fe;价态越低,氧化性越弱,如S2-<S<SO2。
(3)某些氧化剂的氧化性和还原剂的还原性的大小与下列因素有关。
①温度:如热的浓硫酸的氧化性比冷的浓硫酸氧化性要强;热的浓盐酸的还原性比冷的浓盐酸的还原性要强。
②浓度:如硝酸的浓度越大其氧化性越强;
浓盐酸的还原性强于稀盐酸。
③酸碱性:如硝酸根在中性或碱性时几乎无氧化性,在酸性条件下有较强的氧化性。
同主族从上到下,核电荷数递增,元素的非金属性减弱,单质的氧化性减弱,元素的金属性增强,单质的还原性增强,单质的氧化性越强,对应的阴离子的还原性越弱;同周期从左向右,主族元素的金属性减弱,非金属性增强。
声明:本文由北京高考在线团队(微信公众号:bjgkzx)排版编辑,内容来源于网络,如有侵权,请及时联系管理员删除。




































